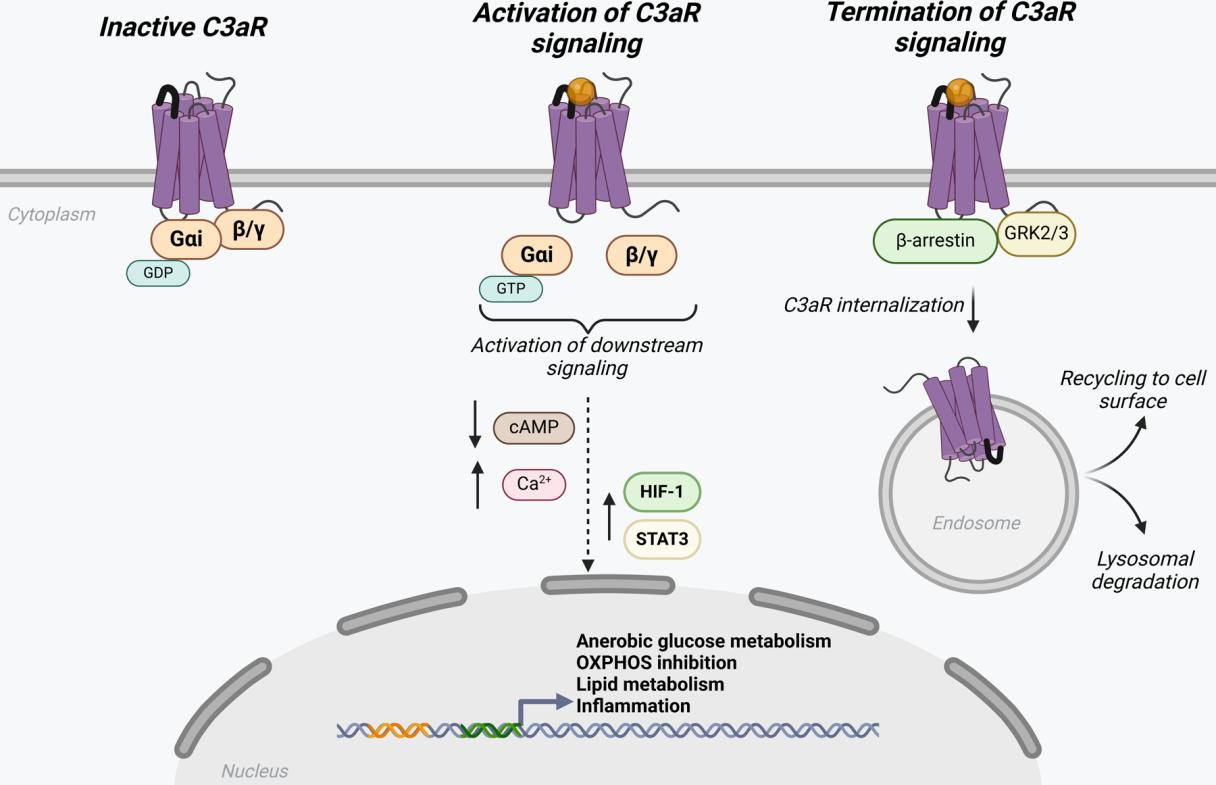
雌激素受体(ER)细胞模型
发布时间:2025/10/17分类:技术文章来源:科佰生物
作为全球第一大癌种的乳腺癌,每年新发病例每年超300万。在乳腺癌患者中,约70% 为雌激素受体(estrogen receptor,ER)阳性、人表皮生长因子受体2阴性(HER2-)。在中国,乳腺癌的发病率也呈现逐年上升的趋势。传统的内分泌治疗通过抑制雌激素的合成或阻断ER的活性来抑制肿瘤生长。雌激素受体调节剂(selective estrogen receptor modulator,SERM)他莫昔芬(tamoxifen),芳香化酶抑制剂(aromatase inhibitors, AI)如来曲唑、阿那曲唑等,雌激素受体降解剂(selective estrogen receptor down-regulators or degraders,SERD)氟维司群(fulvestrant)等是乳腺癌内分泌治疗的基本药物。
但部分患者会因内分泌治疗耐药出现肿瘤复发、进展。耐药通常由多种机制驱动,ERα 编码基因ESR1突变是常见的原因之一。因此ER是乳腺癌药物研究中一个重要靶点。
雌激素受体及其信号通路
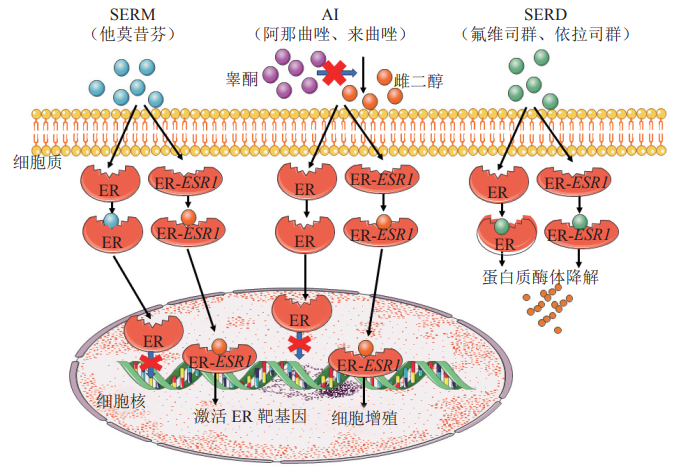
雌激素受体ER属于核受体超家族,是配体依赖的转录调节因子。研究表明,ER在所有脊椎动物及部分无脊椎动物体内均有表达。ER 位于细胞膜、细胞质或细胞核,根据ER所在位置的不同可分为两大类:一类是位于细胞核内的ER,其被称为经典的核受体,包括ERα和ERβ,它们可通过对特异性靶基因的转录的调控发挥生物学效应;第二类为位于质膜的膜性受体,包括经典核受体的膜性成分及G蛋白偶联受体家族的GPR30(GPER-1)、Gaq-ER和质膜相关的ER(ER-X),它们可通过第二信使调控基因转录,间接地发挥生物学效应。
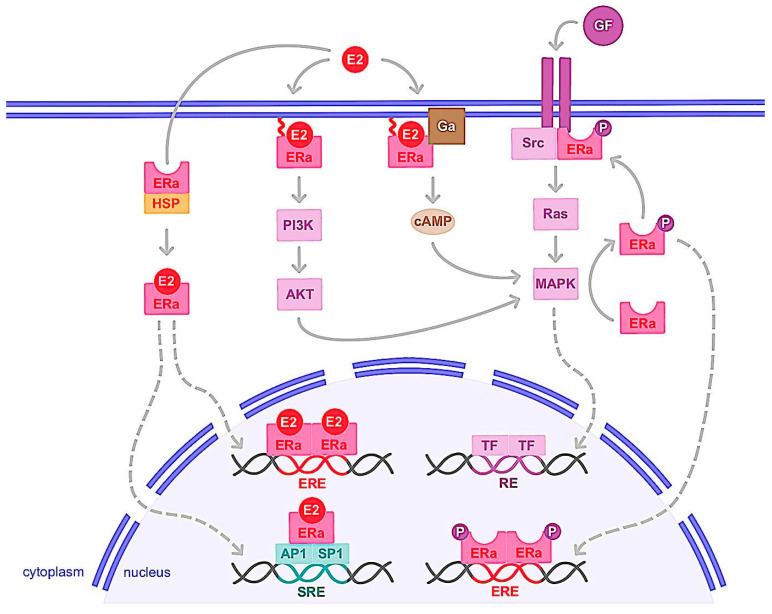
当雌激素(E2)结合或经细胞激酶磷酸化后,ERα在生长因子受体刺激下被激活并转位至细胞核。在那里,ERα同源二聚体通过雌激素反应元件(EREs)直接或间接结合DNA,或与AP1、SP1等其他转录因子结合,后者通过血清反应元件(SREs)与DNA相互作用。这即为ERα的基因组作用,可调控靶基因转录。ERα还可锚定于膜上并与G蛋白(Ga)或GF受体相互作用。ERα激活进而参与第二信使(如cAMP)生成及PI3K/AKT或Ras/MAPK等信号通路的激活。这种非基因组作用最终导致转录因子激活,参与细胞增殖与存活的调控。
ER和乳腺癌
在过去的几十年中,ER在前列腺癌、结肠直肠癌和乳腺癌等各种癌症中的作用已被深入研究。研究表明,雌激素受体不仅会介导乳腺癌的发生,而且在许多其他的人类病理(如心血管疾病、骨质疏松症和肥胖、阿尔兹海默症、自身免疫性甲状腺疾病)中发挥作用。
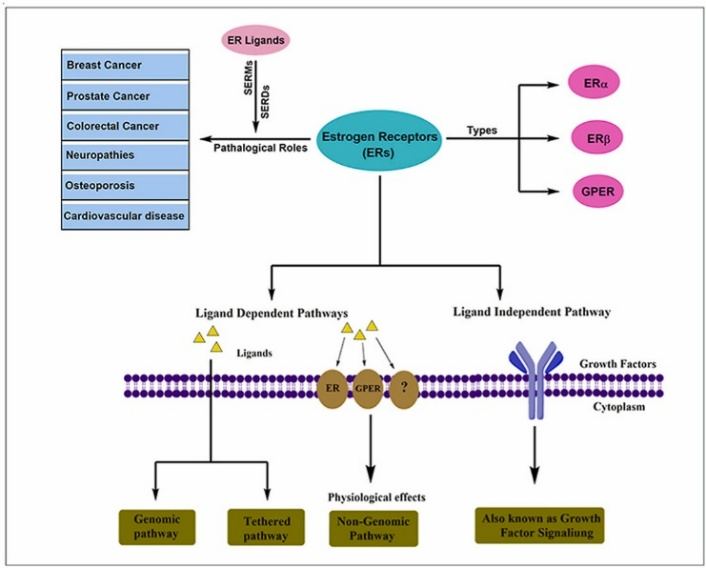
雌激素受体ER高度参与内分泌活动和紊乱,并在乳腺和子宫中起着至关重要的作用。研究表明,ERα在正常乳腺上皮中的表达率不超过10%,但在乳腺肿瘤中约占50%~80%。此外,ERβ的表达与人类乳腺肿瘤中细胞增殖标志物Ki67和细胞周期蛋白A升高有关,ERβ的水平在正常乳腺组织中较高,并且随着肿瘤从早期浸润肿瘤发展为肿瘤而降低。在人乳腺癌细胞系MCF-7中,ERα的DBD结构中Arg260的甲基化可以触发含有ERα、SRC、黏附激酶FAK和磷酸肌醇3-激酶PI3K的p85亚基的细胞质复合物的形成,以响应雌二醇E2。随后这个大分子复合物激活下游丝氨酸/苏氨酸激酶AKT信号通路,导致细胞增殖和细胞存活。
晚期乳腺癌患者内分泌治疗常存在耐药,耐药通常由多种机制驱动,ERα编码基因 ESR1 突变是常见的原因之一。晚期乳腺癌患者经芳香化酶抑制剂(AI)治疗后,约20% ~ 40%患者出现 ESR1 突变,其发生率因转移灶位置而异。ESR1突变多位于配体结合结构域,最常见的突变类型是D538G和Y537S。ESR1 配体结合域突变后,无需雌激素也可激活 ER 及其信号通路。在临床前研究中,氟维司群对 ESR1 突变体较野生型敏感性显著下降。因此,开发能够克服耐药问题的新药物,一直是乳腺癌治疗领域的研究重点。
ER的细胞模型
从他莫昔芬、芳香化酶抑制剂到氟维司群,传统疗法逐渐暴露出耐药性、注射给药不便等局限性。新一代口服选择性雌激素受体降解剂(SERD)以创新作用机制和口服优势,有望重塑HR+/HER2-乳腺癌的治疗格局。另外,还有降解 ER的PROTAC等药物在研发中。以下为部分已上市或处于临床阶段的药物信息:
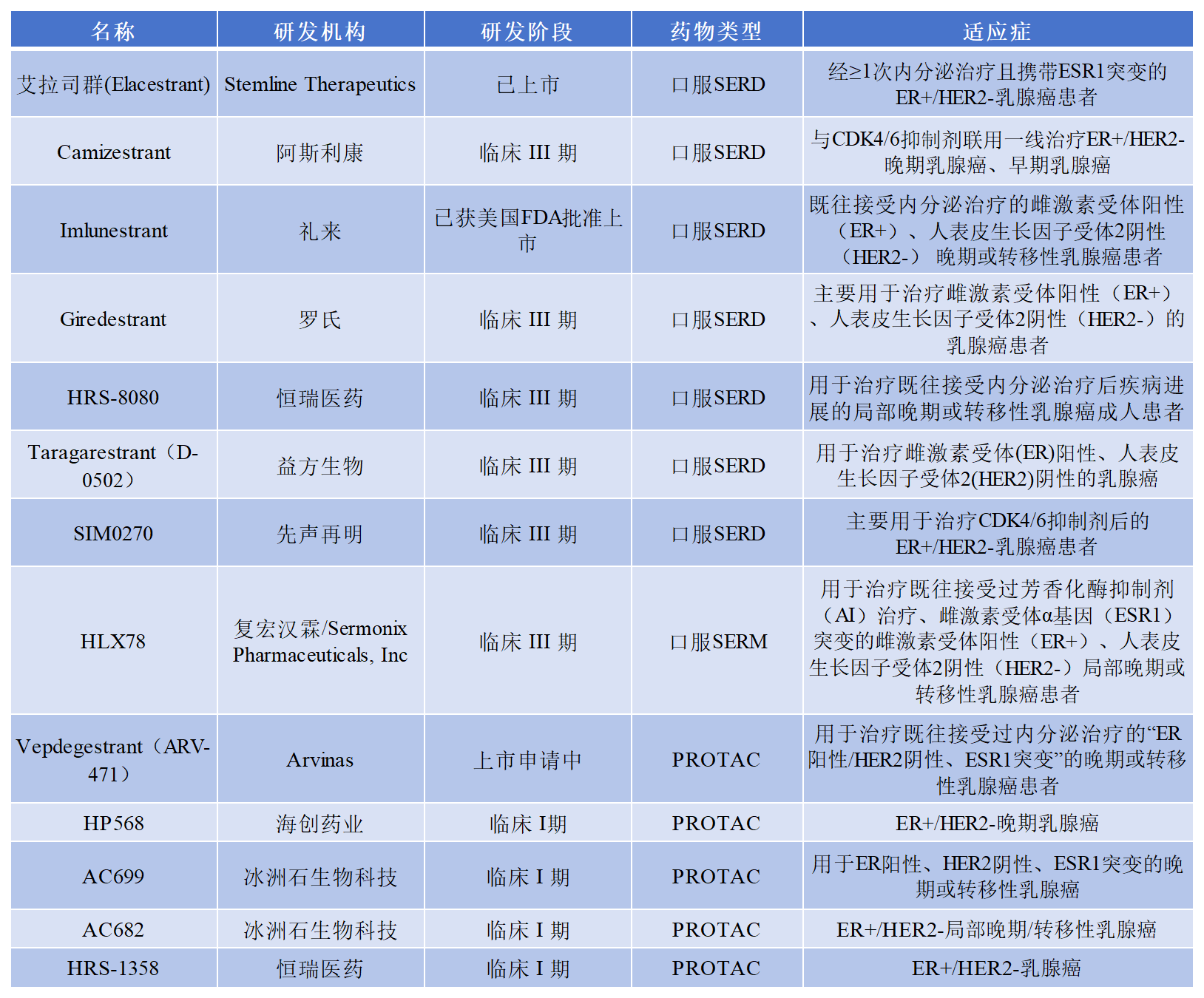
为了助力ER药物的研发,科佰生物开发了基于ESR1信号通路的一系列ER细胞模型,用于候选药物早期机理研究。
细胞产品列表如下:
| Name | Catalog ID |
| ESR1[D538G](Homozygous,AF%:100) Isogenic MCF7 | CBPM0013 |
| ESR1[D538G](Heterozygous,AF%:66.7) Isogenic MCF7 | CBPM0014 |
| ESR1[E380Q](Homozygous,AF%:100) Isogenic MCF7 | CBPM0015 |
| ESR1[Y537C](Homozygous,AF%:100) Isogenic MCF7 | CBPM0017 |
| ESR1[Y537N](Homozygous,AF%:100) Isogenic MCF7 | CBPM0018 |
| ESR1[Y537S] Isogenic MCF7 | CBPM0005 |
| ESR1-GAL4 Luciferase Reporter HEK293 | CBPM0002 |
| ESR1[Y537S]-GAL4 Luciferase Reporter HEK293 | CBPM0003 |
| ESR1[D538G]-GAL4 Luciferase Reporter HEK293 | CBPM0004 |
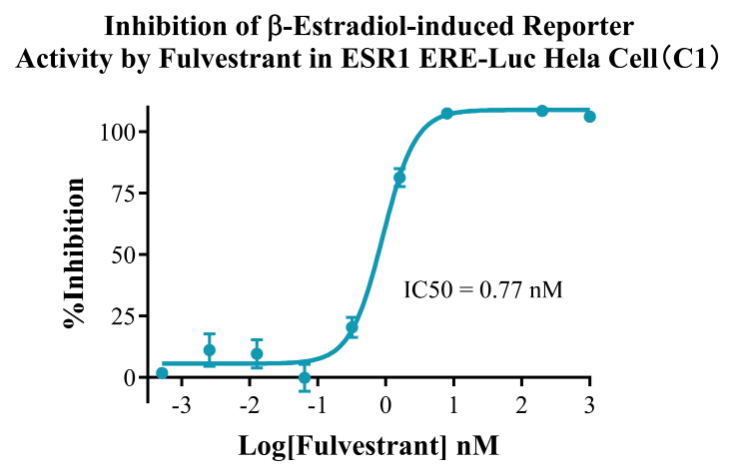
| ESR1 ERE-Luc Hela Cell | CBPM0012 |
| MCF7/FR | CBP60380DR-1 |
| MCF7/TR | CBP60380DR-2 |
部分结果如下:
ESR1[D538G](Homozygous,AF%:100) Isogenic MCF7 CBPM0013
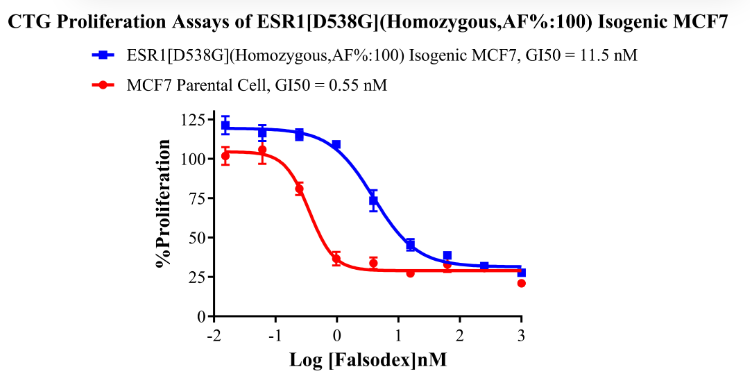
Figure 4. CTG Proliferation Assays of ESR1 [D538G](Homozygous,AF%:100) Isogenie MCF7.
ESR1[D538G](Heterozygous,AF%:66.7) Isogenic MCF7 CBPM0014
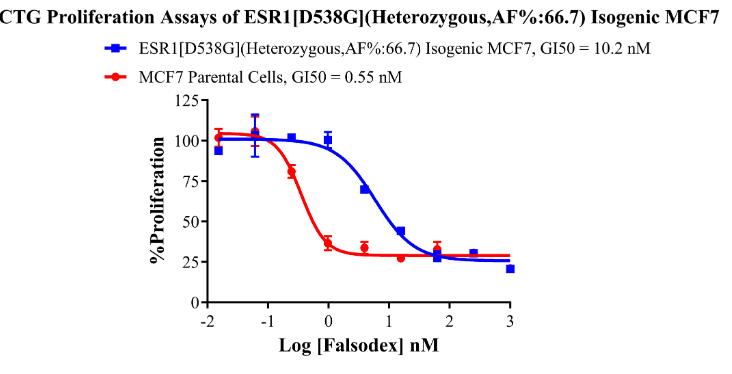
Figure 5. CTG Proliferation Assays of ESR1 [D538G](Heterozygous,AF%:66.7) Isogenie MCF7.
ESR1[E380Q](Homozygous,AF%:100) Isogenic MCF7 CBPM0015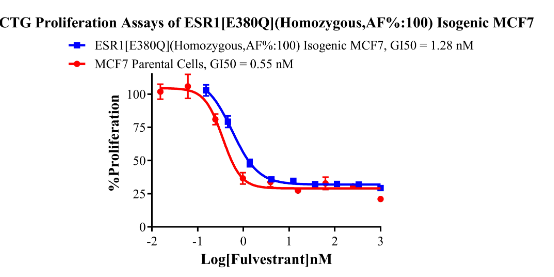
ESR1[Y537C](Homozygous,AF%:100) Isogenic MCF7 CBPM0017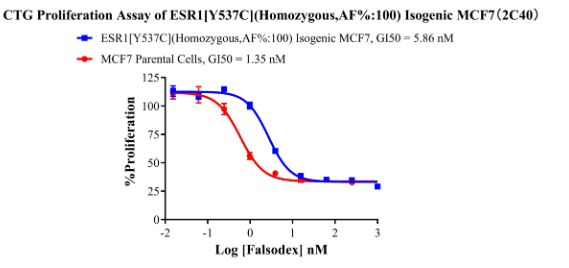
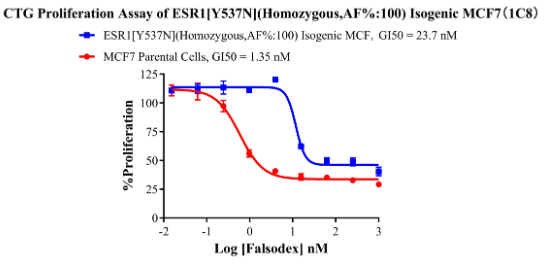
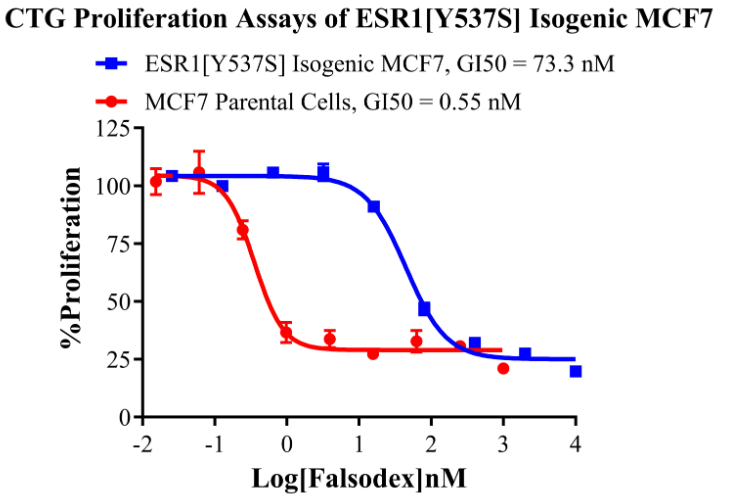
ESR1[Y537S] Isogenic MCF7 CBPM0005